�п�Ժ�K�ݼ{�����S��������3D��ӡ���Ƥ�w֧�ܣ���������ϴ��������h��
�S���˿����g�������Բ�������������������ֲ�������l���У������w��ȱ�ɞ��R���t�W���R�ľ����𡣽M�����������������������3D�����ӡ���g�ɘ���ģ�M���w�����ĽM������֧�ܣ�Ȼ������lչ������ȱ�����m������īˮ�����y���ˮ���z�������̖����ģʽ��ƥ�䡢�ɴ�ӡ�Բ�������Դ�Ȇ��}���x�ӌ��ˮ���z�m���������w�M�����̖��������Ҳ���R�ͼ������Ժ߷������y�Լ��������
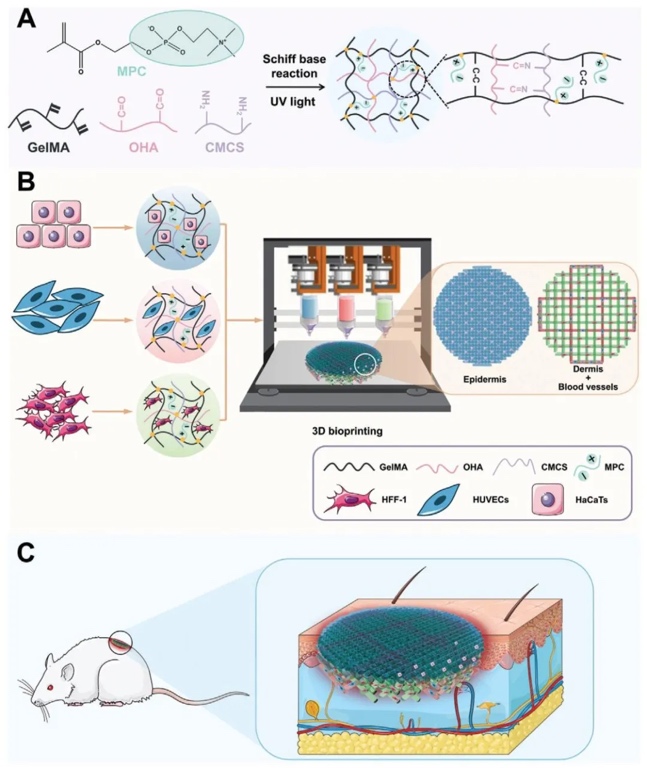
�Ї��ƌWԺ�K�ݼ{���g�c�{�����о������S���о��T�F��_�l��һ�N�����x�ӌ�늷�������īˮ��GHCM����������3D�����ӡ���g�Ƃ��p�ӌ��Ƥ�w֧������ȫ��Ƥ�wȱ�p�ί���ԓ����īˮ�����z����ϩ������GelMA�����������|�ᣨOHA�����ȼ������ǣ�CMCS����2-����ϩ�����һ�����đ�A��MPC���M�ɣ���Q�˂��y���ˮ���z���T�����}�����P������ “3D Bioprinting of Double�\Layer Conductive Skin for Wound Healing” ���}�l���ڡ�Advanced Healthcare Materials���ϣ���늻��ԽM���ľ��_���̺������t�W�����ṩ���²��ԡ�

�����
1. GHCM����īˮ/ˮ���z���Ƃ��c����
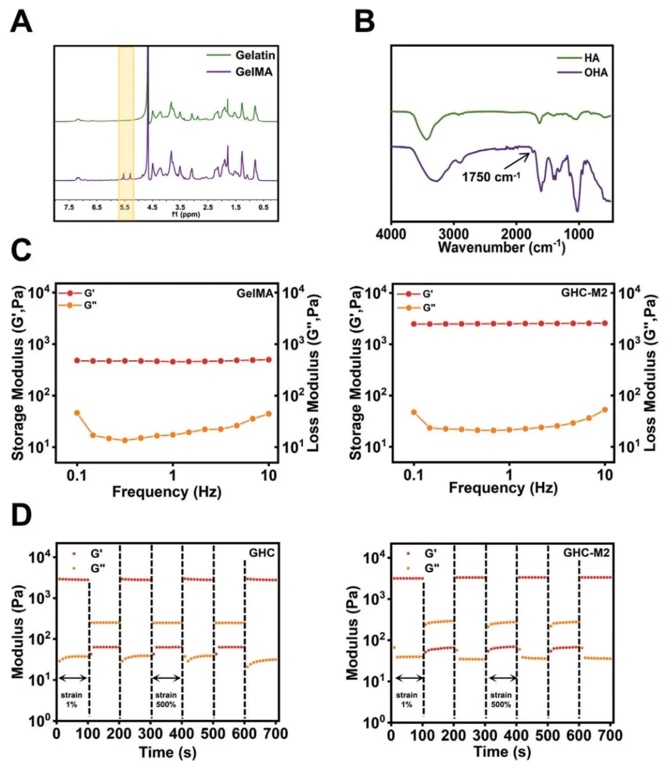
ͨ�^���W�ϳɡ����V�������������ܜyԇ���о��������о�����GelMA��OHA��CMCS��MPC�M�ɵ�GHCM����īˮ��ˮ���z���Y��������ԓ����īˮ��4°C��Ϻ�l�����z - ���z�D׃����UV���տ��γɷ���ˮ���z���䃦��ģ����0.1 - 10Hz�l�ʷ������h���ړp��ģ������ȫ������ģ��ֵ�s3kPa���c��ȻƤ�w�ஔ��ͬ�r��ˮ���z�������õ��������ԡ�����ԡ������Ժ����������ԣ�MPC�������@�������ˮ���z���x��늌��ʣ���GHC - M2ˮ���z�C��������ѡ�
2. GHCM����īˮ�Ŀɴ�ӡ��
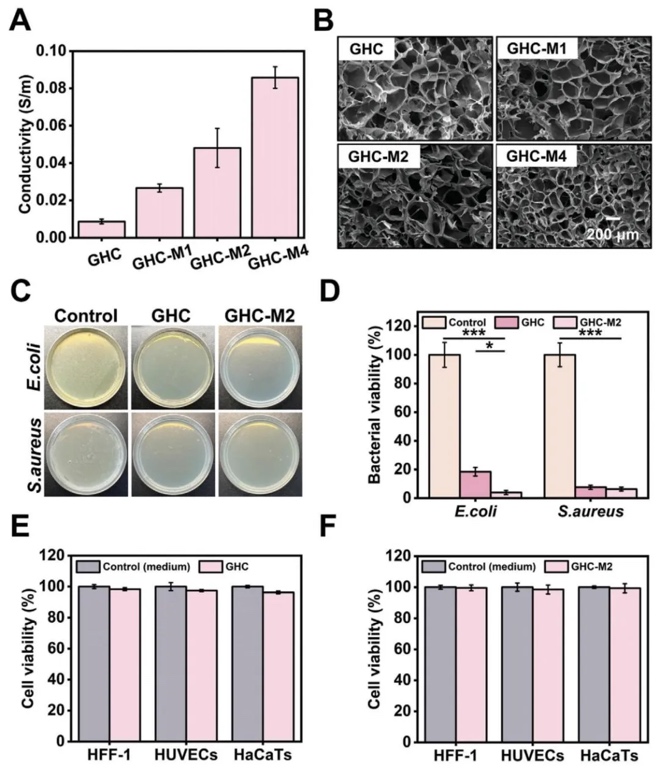
������׃�yԇ����ӡ���������ԙz�y���о��������о���GHCM����īˮ��3D��ӡ�е����ܡ��Y���@ʾ��OHA��CMCS�ļ������������īˮ��ճ�ȣ�MPC�ē��s�Mһ��������ԓ���ܣ�GHC - M2����īˮ�����@���ļ���׃ϡ�О�Ϳ����|׃�ԣ����ڴ�ӡ��֧�ܽY����������ӡ���zֱ���ӽ��˜ʇ���ֱ������ӡ��ֵ���_0.93 ± 0.05�����⣬������GHC - M2����īˮ��ӡ��֧���д���ʸߣ���ֳ���ã��C����ӡ�^�̺�UV���Ռ��������Ժ���ֳ�o���@����Ӱ푡�
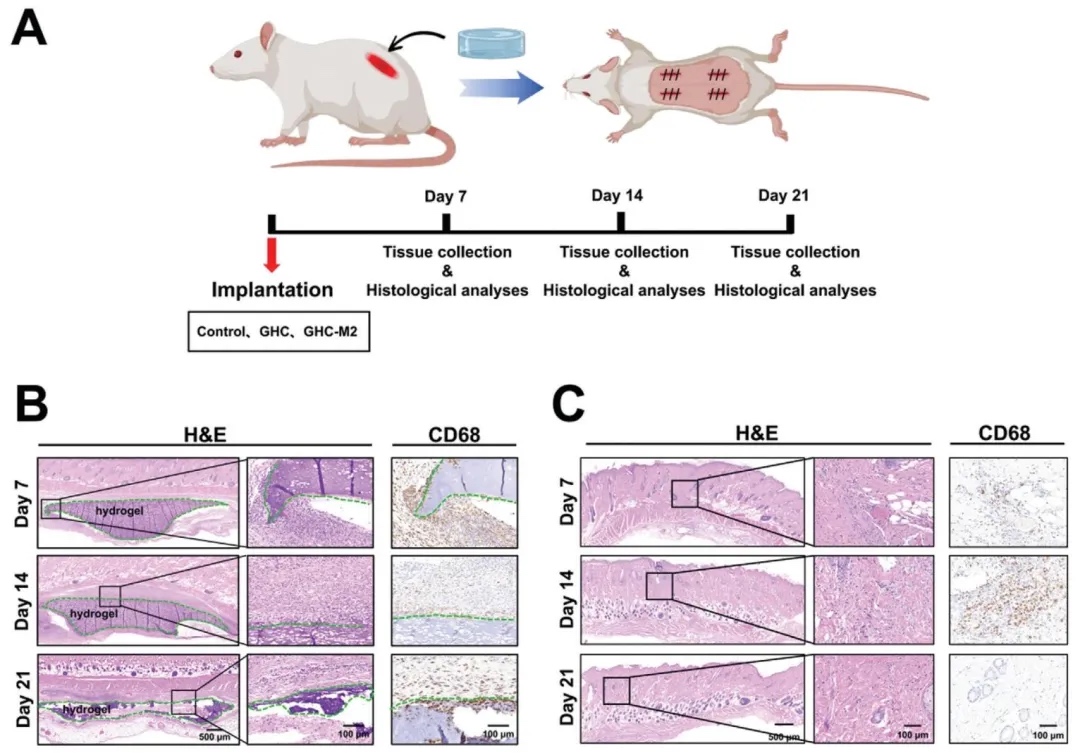
3. GHCMˮ���z���w�����������Ժͽ���
ͨ�^����M���WȾɫ���о���������Sprague - Dawley��SD��������о������u��GHC - M2ˮ���z���w�����������Ժͽ�����r���Y��������ֲ��ˮ���z������������ã�7��rˮ���z�܇����������࣬���F�����װY���������S���r�g���L�װY��u�p�p��21��r�c���սM�M���ΑB���ƣ��Ҵ˕rˮ���z���ѽ��⣬�����������併�������cƤ�w��������ƥ�䣬�f��GHC - M2ˮ���z�m���w�ȑ��á�
4. �p�ӌ��Ƥ�w֧�ܵ�3D��ӡ���w����u��
�\��3D��ӡ���g�����������ߟɹ�Ⱦɫ���о���������3D��ӡ���p�ӌ��Ƥ�w֧���M���w����о����Y���l�F��ԓ֧���ܴ��M��Ƥ������HaCaTs���w�ơ����w�S������HFF - 1���̓�Ƥ������HUVECs����ֳ�c�w�ƣ�����Ѫ�ܻ�����Ƥ���M�̡����磬GHC - M2�M��HaCaTs������������e��24h���@���pС��HFF - 1��HUVECs��21d�r�����w������Ƥ����GHC - M2�MѪ�ܳ����ӛ��CD31���_���ߣ���Ƥ�Y�������ӛ��CK10���_Ҳ�@�����ڌ��սM��

5. �p�ӌ��Ƥ�w֧�ܵ��w���ޏ�Ч��
���Ä���ģ�͌��M���W�������о���������SD����ȫ��Ƥ�wȱ�pģ�͞��о������u���p�ӌ��Ƥ�w֧�ܵ��w���ޏ�Ч�����Y���@ʾ��ֲ���p�ӌ��Ƥ�w֧�ܣ�GHC - M2 + cell�M���Ă��������ٶ���죬21d�r�����]���ʸ��_98 ± 0.3%��H&EȾɫ��MassonȾɫ�����ߟɹ�Ⱦɫ�Y��������ԓ�M���M����ѿ�M���γɡ��zԭ���e��Ѫ�����ɣ�����������Ƥ���^�̣���Ч�ؽ�������Ƥ�w�Y����ʹ����ӽ���ȻƤ�w��
�о��YՓ
���о��_�l��һ�N���µ�3D�����ӡ���ԣ�ͨ�^�x�ӌ�늷�������īˮ���ܼ��������˾���������Ե��p�ӌ��Ƥ�w֧�ܡ�ԓ3D��ӡ֧���^�����^ģ�M����Ȼ�M�������H�鼚�������L���w�ƺͷֻ��ṩ���m�˵Č���h����߀���������wƤ�w�Ķ��ӽY���ͼ������g�ֲ�����ȫ��Ƥ�w���ڴ���ģ���У��@�N֧�܌��F�˿��ٸ�Ч��Ƥ�w������δ���������@�N�����x�ӌ������īˮ��3D��ӡ���g���������������ඨ�ƻ��������ԵĻ����٣����ڽM�������I��
����Դ��
https://doi.org/10.1002/adhm.202404388
(؟�ξ���admin)
��һƪ��Royal3D�Ƴ����ͺ�����ShearWaterˮ�o�˙C�����Ì���LFAM��ˇ����
- ��Royal3D�Ƴ����ͺ�����ShearWaterˮ
- ���п�Ժ�K�ݼ{�����S��������3D��ӡ���
- �������ļ��g��W�cVIT�����_�l3D��ӡ��
- ��Revo Foods�Ƴ�������Ƴɵ�EL BLANCO
- ���W��Ͷ�Y3D��ӡ�۽�Ĥ�Ŀ��KeratOPrin
- ��3D��ӡЬ���N���~400��600�f����ӭ��
- ��BellaSeno ��˾�Ƴ�ȫ�µ�3D��ӡ����ֲ
- �������VTOL Vertiia ��ʹ�� Conflux ��
- ��3D��ӡ�ǰͿ˿��ȵ�����¿��_˹�ݣ���
- �����ݴ�W���S˹��У�_�l��3D��ӡ���g
- ��3D��ӡ��������3D��ӡ�P���������ij���
- ����3D��ӡ�C�����b���ˣ�����3d��ӡ��һ
- ���Լ�������һ�_ֻ��20��Ԫ��3D��ӡ��
- ���P�c3D��ӡ���ޏ�������E�еĽ��䰸��
- ���֙C��ע���ˣ��Ø�ݮ��+3D��ӡ�C����
- ���D�⣺3D��ӡ�������a����
- ��SOLS��˾�l���ɶ��Ƶ�3D��ӡ�C��Ь�|
- ��ӯ��3D��ӡ�������䰸������
- ��10�����ص�3D��ӡ���裬����һ������ϲ
- ��3D��ӡ���҃��b�đ��ã��cȼ�㌦���g


 Royal3D�Ƴ����ͺ�����S
Royal3D�Ƴ����ͺ�����S �����ļ��g��W�cVIT����
�����ļ��g��W�cVIT���� Revo Foods�Ƴ�������Ƴ�
Revo Foods�Ƴ�������Ƴ� �W��Ͷ�Y3D��ӡ�۽�Ĥ�Ŀ
�W��Ͷ�Y3D��ӡ�۽�Ĥ�Ŀ 3D��ӡЬ���N���~400��600
3D��ӡЬ���N���~400��600 3D��ӡ���F��̶�
3D��ӡ���F��̶� �炐�ȁ���W����
�炐�ȁ���W���� ʧȥ1/3����,���
ʧȥ1/3����,��� 3D��ӡܛƤ�|����
3D��ӡܛƤ�|���� 3D��ӡ��Q������
3D��ӡ��Q������ ���ܲ����¡����T
���ܲ����¡����T

